Entre os parâmetros que interferem na reação de esterificação encontra-se o tipo de catalisador utilizado (OLIVEIRA et al, 2014). Argilominerais podem ser utilizados como catalisadores na reação de esterificação. A classe das esmectitas (montmorilonita) estão entre as mais usadas para fins catalíticos. Na etapa de reação, a argila montmorilonita pode ser facilmente separada por filtração, pois não se dissolve no meio reacional (OLIVEIRA et al, 2014). Lembre-se que um catalisador não é consumido durante a reação, sendo regenerado ao final do processo. A argila pode ainda ser reutilizada como catalisador em outra reações (OLIVEIRA et al, 2014).

Construindo a Estrela Verde
Para construir a Estrela Verde leia com atenção os passos a seguir.

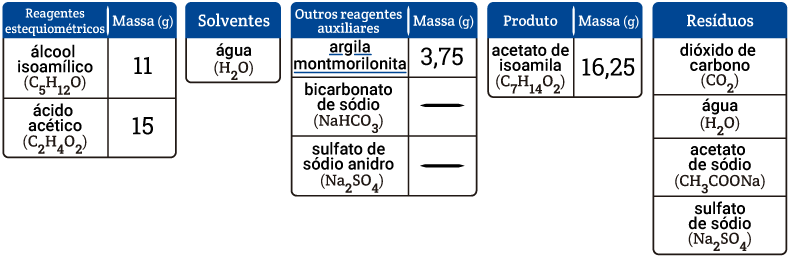
Em um balão de fundo redondo, adicionar 0,125 mol de álcool isoamílico, 0,250 mol de ácido acético e 3,75g de catalisador argila montmorilonita. O condensador de refluxo foi adaptado e a mistura de reação aquecida durante 2 horas em banho de óleo na temperatura de ebulição do álcool correspondente. Após 2 horas de aquecimento, deixe a mistura reacional esfriar à temperatura ambiente.
Após 2 horas de aquecimento, foi feita uma filtração simples para remoção do catalisador argila montmorilonita e colocou-se a mistura de reação em um funil de separação, adicionando-se cuidadosamente 100 mL de água. A fase aquosa (inferior) foi desprezada e a fase orgânica foi lavada 2 vezes com 50 mL de solução saturada de bicarbonato de sódio. Desprezou-se novamente a fase aquosa e lavou-se a fase orgânica com 25 mL de água. O éster bruto foi transferido para um béquer, ao qual se adicionou sulfato de sódio, com objetivo de remoção da água. Posteriormente, uma filtração foi realizada. OBS: A remoção do excesso de ácido acético do meio reacional é realizada através da adição de bicarbonato de sódio. Ao adicionar bicarbonato de sódio a fase orgânica ocorre a liberação de gás, indicando a formação de dióxido de carbono. Com a adição de bicarbonato, também observa-se a formação de água e acetato de sódio. Sulfato de sódio é resíduo proveniente do uso como agente secante.
C5H12O + C2H4O2 = C7H14O2 + H2O
Para escolher os códigos de perigo no simulador, é preciso abrir o pdf da ficha de segurança. Na ficha de segurança, os códigos de perigo estão destacados na seção 2.2. As fichas de segurança fornecem informações sobre os perigos das substâncias químicas.
| Álcool Isoamílico (FISPQ) | Acetato de Sódio (FISPQ) | Sulfato de Sódio (FISPQ) |
| Ácido Acético (FISPQ) | Bicarbonato de Sódio (FISPQ) | |
| Argila montmorilonita (FISPQ) | Acetato de Isoamila (FISPQ) |
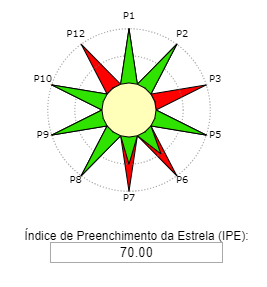
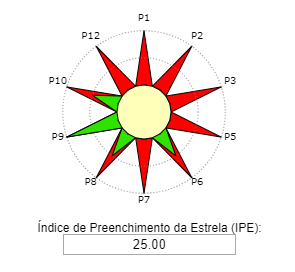
Os princípios P1, P3, P5 e P12 são preenchidos automaticamente.
Avaliar o restante dos princípios (P2, P6, P7, P8, P9, P10 ) de acordo com o roteiro experimental. Informações sobre degradabilidade e renovabilidade podem ser obtidas nas fichas de seguranças dos produtos químicos.
Para debater
Após construir e comparar a sua Estrela Verde reflita sobre a pergunta a seguir:
A atividade econômica de exploração da argila pode causar algum dano ao meio ambiente?
Referências
OLIVEIRA, C. A., et al. Síntese de Esteres de Aromas de Frutas: Um Experimento para Cursos de Graduação dentro de um dos Princípios da Química Verde. Revista Virtual de Química, v.6, n.1, p.152-167, 2014.
Anterior


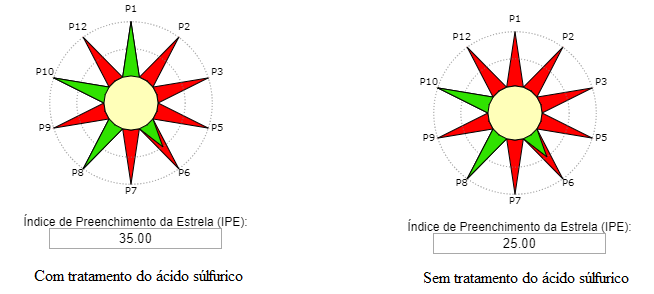

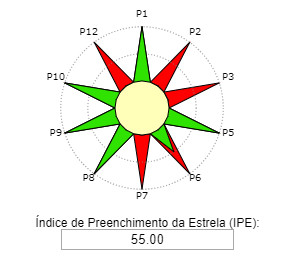




 Reação. Em um balão de fundo redondo, adicionar 0,125 mol de álcool isoamílico, 0,250 mol de ácido acético e 0,05mL de catalisador H2SO4. O condensador de refluxo foi adaptado e a mistura de reação aquecida durante 2 horas em banho de óleo na temperatura de ebulição do álcool correspondente. Após 2 horas de aquecimento, deixe a mistura reacional esfriar à temperatura ambiente.
Reação. Em um balão de fundo redondo, adicionar 0,125 mol de álcool isoamílico, 0,250 mol de ácido acético e 0,05mL de catalisador H2SO4. O condensador de refluxo foi adaptado e a mistura de reação aquecida durante 2 horas em banho de óleo na temperatura de ebulição do álcool correspondente. Após 2 horas de aquecimento, deixe a mistura reacional esfriar à temperatura ambiente.